 |
Российская Ассоциация
(РАМЛД) |
г.Москва, 119526, а/я 117, РАМЛД,
т/ф.: (495) 433-24-04
|
автор: Д.В.Фадин фирма ОМБ год издания: 2003 |
Роль преаналитического этапа в стандартизации лабораторных исследований
Как известно, процедура лабораторного исследования подразделяется на преаналитический, аналитический и постаналитический этапы. К сожалению, большая часть усилий по стандартизации сосредоточена на аналитическом этапе. При этом не учитывается тот факт, что именно на аналитическом этапе количество операций непосредственно во время анализа минимально, а средства контроля качества наиболее развиты и реально применяются в практике российских лабораторий, в то время как для преанатического этапа такие меры контроля не разработаны. Преаналитический этап в наименьшей мере находится под контролем лаборатории, так как значительная его часть осуществляется сотрудниками других подразделений ЛПУ. Преаналитический этап включает назначение анализа, взятие биоматериала, транспортировку, пробоподготовку – те операции, которые на сегодняшний день стандартизованы в минимальной степени. По самым разным литературным источникам доля ошибок преаналитического этапа в общем числе лабораторных ошибок составляет не менее 50%. На долю аналитического этапа приходится не более 20% ошибок, при этом значительная часть этих ошибок в первую очередь связана с отсутствием стандартов на выполнение различных операций преаналитического этапа или с тем, что эти стандарты игнорируются персоналом ЛПУ. В настоящее время разработана лишь незначительная часть протоколов по назначению лабораторных исследований при разных нозологиях. В различных ЛПУ применяются различные методики взятия биоматериала, причем влияние способа взятия биоматериала на результат игнорируется. Понятие качества преаналитического этапа активно обсуждается в последние годы, однако из-за отсутствия нормативной базы и технических методов контроля реальные меры к обеспечению качества не применяются. В то же время зарубежная практика показывает, что именно стандартизация преаналического этапа обеспечивает резкое снижение лабораторных ошибок. Основой для принятия таких стандартов могут стать современные системы взятия биоматериала.
Выбор биоматериала для проведения исследований является одним из определяющих факторов для адекватного сравнения результатов, полученных в разное время и в различных лабораториях. В табл.1 представлены различия значений аналитов при использовании сыворотки или плазмы для проведения биохимического анализа.
Таблица 1. Различие концентрации аналитов в сыворотке и плазме крови.
|
Аналит |
Различие концентрации аналита в сыворотке и плазме крови, % |
Основная причина различия |
|
Калий |
+ 6,2 |
Выход из клеточных элементов |
|
Неорг. фосфат |
+10,7 |
Выход из клеточных элементов |
|
Общий белок |
-5,2 |
Эффект фибриногена |
|
Аммиак |
+38 |
Выход из клеточных элементов, гидролиз глутамина |
|
Лактат |
+22 |
Выход из клеточных элементов |
Стандартизация биоматериала для проведения исследований позволит в значительной мере сократить количество ошибок, связанное с неадекватным выбором; решить часть проблем с установлением референсных значений.
Взятие венозной крови в наименьшей степени контролируется руководством лаборатории. Зачастую выбор материалов для взятия крови осуществляется персоналом ЛПУ без учета требований лабораторий, что вынуждает отбраковывать значительную часть образцов. В настоящее время взятие венозной крови осуществляется одноразовым шприцем или толстой иглой в стеклянную или пластиковую пробирку или вакуумными системами промышленного производства. В первом случае взятие крови зависит от квалификации персонала и не может быть стандартизировано. Применение вакуумных систем, конечно, не может полностью гарантировать от ошибок во время процедуры венопункции, однако позволяет в наибольшей мере обеспечить единообразие образцов. Число случаев гемолиза, микросгустков в образце венозной крови значительно увеличивается при двухкратном прохождении крови через иглу шприца под давлением. При контакте пробы с воздухом возможна ее контаминация. Отбраковка таких образцов в лаборатории в настоящее время осуществляется только при визуальном контроле. Два года назад на европейском рынке появился первый прибор, позволяющий в автоматическом режиме выявлять образцы с микросгустками, гемолизом и т.п., однако высокая стоимость ограничивает его применение в практике российских лабораторий. Качество образца в значительной мере определяет точность работы приборов на аналитическом этапе исследования. Несмотря на то, что соотношение крови и антикоагулянтов общеизвестно, на практике оно часто не соблюдается. Это происходит из-за того, что при ручном дозировании не представляется возможным точно соблюдать необходимое соотношение крови и реагента, и, кроме того, персонал процедурных кабинетов не представляет себе последствий нарушения регламента взятия. Единственная возможность поддержания необходимого соотношения - использование систем с промышленно созданным вакуумом. Такие системы забирают строго указанный на пробирке объем крови и имеют на этикетке риску, позволяющую лаборантам визуально контролировать соблюдение объемных требований.
Во многих странах взятие капиллярной крови для лабораторных исследований ограничено применением в неонаталогии и педиатрии. Это связано в первую очередь с тем, что при взятии образец содержит смесь капиллярной крови, обломков клеток, межклеточной жидкости и т.п. В этой связи представляется важным использование автоматических скарификаторов, гарантирующих низкую травматичность и соблюдение нужной глубины прокола, в зависимости от типа скарификатора. Во многих лабораториях при взятии гематологических проб капиллярной крови считается допустимым нарушать соотношение крови и ЭДТА, что приводит к искажению количества тромбоцитов при подсчете в автоматических анализаторах.
К получению пробы мочи ряд лабораторий предъявляет пониженные требования. Использование домашней посуды вместо специальных контейнеров и пробирок приводит к контаминации проб, получению заведомо ложных результатов и невозможности стандартизации.
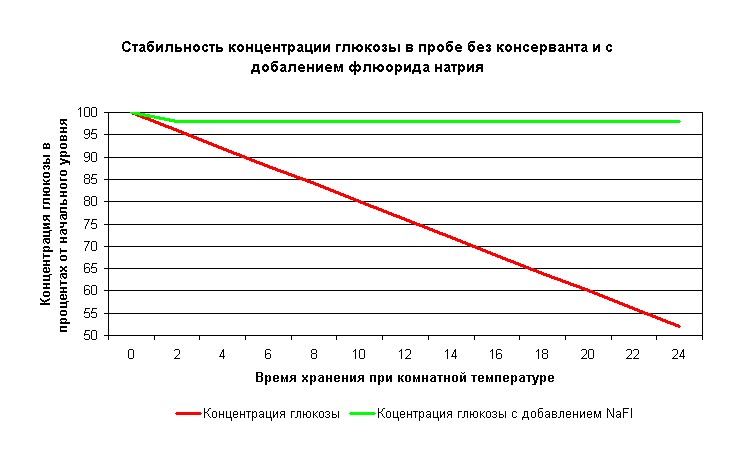
Одной из главных проблем является игнорирование влияния сроков постановки лабораторных тестов и правил транспортировки проб в лабораторию. К примеру, значительная часть расхождений между автоматизированным и микроскопическим подсчетом клеточных элементов вызвана несоблюдением сроков постановки тестов. Стандартизация сроков доставки и жесткое соблюдение стандартов позволит избежать ошибочных результатов. Перевозка крови в стеклянных пробирках с ватными пробками приводит к впитыванию крови в ватный тампон, гемолизу и т.п. Перевозка проб, предназначенных для биохимического или иммунологического анализа без предварительного центрифугирования, приводит к искажению результатов за счет влияния клеточных элементов. Одним из решений, позволяющих облегчить транспортировку и увеличить сроки постановки реакций, является применение стабилизаторов и разделительных элементов, например гелей и гранул. Примером может послужить стабильность глюкозы в пробах при наличии или отсутствии стабилизатора в образце.
Первым этапом, который осуществляется непосредственно в лаборатории, является пробоподготовка. Основной ошибкой при центрифугировании является применение в протоколах пробоподготовки показателя скорости вращения центрифуги вместо относительной центрифужной силы, которая расчитывается по формуле ОЦС = 1.118 x радиус (об/мин/1000)² и зависит от радиуса используемой центрифуги. Другим источником ошибок на этапе пробоподготовки является аликвотирование проб – сыворотка разливается из первичной пробирки в одну или несколько вторичных. Полная стандартизация этого этапа возможна только при наличии в лаборатории анализаторов, работающих с первичными пробирками.
Таким образом, при стандартизации преаналитического этапа следует не только исключить ошибки, но и соблюдать ряд общих требований:
· требования к стандартизации идентификации проб: наличие этикетки на каждой пробирке с биоматериалом и применение лабораторной информационной системы для идентификации проб. Наличие ЛИС – лабораторной информационной системы - позволяет выявить и проанализировать ошибки преаналитического этапа и принять меры для их устранения.
· проведение регулярного мониторинга преаналитического этапа для выявления неверных действий и своевременной корректировки работы персонала.
· применение современных систем взятия материала, имеющих все необходимые сертификаты качества и использование их в строгом соответствии с инструкциями производителей.
· обеспечение безопасности персонала и удобства применения систем взятия биоматериала, в противном случае выработанные стандарты исследований просто не будут соблюдаться персоналом ЛПУ.
Соблюдение правил преаналитического этапа является необходимым для стандартизации результатов лабораторного исследования в целом.
Литература
Samples: From the Patient to the Laboratory. The impact of preanalytical variabled on the quality of laboratory results. W.G. Guder, S. Narayanan, H. Wisser, B.Zawta Git verlag 2001
Обеспечение качества лабораторных исследований. Преаналитический этап. Под редакцией В.В. Меньшикова Москва, Лабинформ 1999.
Медицинские лабораторные технологии. Том 1. Под редакцией Карпищенко А. И. С-Петербург.1998.
|
автор: Д.В.Фадин фирма ОМБ год издания: 2003 |
|




